گزارش کار آزمایشگاه شیمی آلی 1 شامل عنوان های زیر در این نوشته برای شما قابل دانلود است:
حل کردن و صاف کردن
بحث کلی
دستور کار
سوالات
استخراج
بحث کلّی
روش عملی
سوالات
کریستاله کردن مجدد استانیلید بوسیله آب
روش کار
تبلور
تبلور مجدد
تصعید
بحث کلی
روش آزمایش
تجزیه کیفی عنصری ترکیبات آلی
آزمایش ذوب با سدیم (تکلیس با سدیم)
شناسایی هالوژنها
آزمایش نیترات نقره
شناسایی ید
شناسایی برم
شناسایی کلر
شناسایی گوگرد
شناسایی کربن و هیدروژن
شناسایی نیتروژن
سوالات
روی لینک دانلود کلیک کنید و سپس برروی دانلود رایگان کلیک کنید
رمز فایل
www.chemistrymg.parsiblog.com
ید یکی از عناصر ضروری برای بدن است که بدن به مقدار بسیار کم به آن برای هورمون تیروکسین غده ی تیروئید نیاز دارد. در مناطقی که مقدار ید کم است و غذاهای دریایی خورده نمیشود کمبود ید موجب بیماری گواتر و تغییرات در پستان و کرتینیسم و عقبماندگی ذهنی کودکان متولدشده میشود. برای پیشگیری از این بیماری در این مناطق از قرص های حاوی مواد ید دار استفاده میشود یا با افزودن مقادیر خیلی کم پتاسیم یدید یا سدیم یدید یا پتاسیم یدات به نمک خوراکی از این بیماری جلوگیری میشود. غذاهای دریایی منبع ید هستند بنابراین در مناطق کوهستانی با خاک عاری از ید این بیماری ها بیشتر دیده میشود.
آشکارساز وسیله است که حضور برخی از پدیده های فیزیکی را نشان می دهد. آشکارسازهای آشنا عبارتند از فیلم عکاسی برای نشان دادن حضور تابش الکترومغناطیسی یا پرتوزا و سطح جیوه در یک دماسنج برای آشکارسازی تغییرات دما. چشم انسان نیز یک آشکارساز است.چشم تابش مرئی را به علامت الکتریکی تبدیل می کند که از طریق رشته های عصبی در عصب نوری به مغز منتقل می شود.
ترانسدیوسر، نوع خاصی از آشکارساز است که علامت ها را مانند شدت نور،pH ،جرم و دما را به علامت های الکتریکی تبدیل میکند که متعاقبا میتوانند تقویت و دستکاری شده و در نهایت به اعدادی متناسب با برزگی علامت اولیه تبدیل شوند.
ترانسدیوسر نوعی آشکارساز است که انواع مختلف کمیت های شیمیایی یا فیزیکی را به ولتاژ، بار، یا جریان الکتریکی تبدیل می کند.
یکی از مهمترین روشهای تیترسنجی، نوعی از محلول استاندارد یُد به نام واکنشگر کارل فیشر را برای تعیین آب، به ویژه در مواد آلی به کار می برد. واکنشگر کارل فیشر متشکل از یُد، پیریدین و گوگرد دی اکسید به نسبت 1 به 3 به 10 است که در متانول حل شده است. قدرت واکنشگر با میزان یُد آن تعیین می شود. واکنش آن با آب توسط واکنش زیر تشریح می شود:
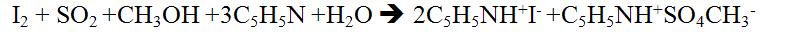
در اینجا یُد به یدید کاهیده و گوگرد دیوکسید به کمپلکسی از یون سولفات اکسید می شود. برای پیشرفت واکنش آب مورد نیاز است. نقطه ی پایانی را می توان با چشم مبتنی بر رنگ قهوه ای واکنشگر اضافی آشکار ساخت، ولی معمولا با اندازه گیری های الکتروآنالیتیکی تعیین می شود. استاندارد کردن متناوب با تیتراسیون محلولهای استاندارد آب در متانول یا سدیم تارتارات تک آبه ی با خلوص استاندارد اولیه انجام می شود.
چند سازنده ی دستگاه، دستگاه های نیم خودکار یا خودکار برای تعیین آب در تعداد زیادی از انواع نمونه ها با تیتراسیون کارل فیشر عرضه کرده اند. تعیین آب با این گونه دستگاه ها، یکی از روش های تجزیه ای متداول در آزمایشگاه های صنعتی است.
در مواردی که تماس اندازه گیر دما با پروسه امکان پذیر نیست مثلا هنگامی که پروسه متحرک است و یا دمای آ بسیار بالاست به گونه ای که هرگونه تماس موجب ذوب شدن و خرابی اندازه گیر دما میشود و یا هنگامی که پروسه دارای مواد مخرب و زیانبار است از اندازه گیر تشعشعی دما (پیرومتر) استفاده میشود. نمونه هایی از اینگونه موارد را می توان در صنایع ریخته گری و فولاد و همچنین صنایع چینی و سرامیک و صنایع شیمیایی پیدا کرد. برای انداز ه گیری دما بدون تماس مستقیم یا غیر مستقیم با پروسه، از اندازه گیرهای تشعشعی و نوری استفاده میشود. مشهورترین نوع پیرومتر disappearing filament است.
در پیرومتر درخشندگی فیلامان لامپ پیرومتر توسط اپراتور با تغییر جریان گذرنده از آن تغییر میکند. از طریق چشمی پیرومتر هم جسم داغ و هم فیلامان لامپ قابل رویت هستند. وقتی که درخشندگی فیلمان با جسم گرم یکی شد فیلامان نامرئی میشود و از طریق جریان برق گذرنده از فیلامان ، دمای جسم گرم اندازه گیری میشود.
حد بالای دمای قابل اندازه گیری با اندازه گیرهای تشعشعی به حدود 4000 درجه سانتی گراد میرسد.

اندازه گیری گرانروی رنگ نه تنها یک آزمایش سودمند است ، بلکه برای کنترل کیفیت محصولات یک عمل ضروری است. بنابراین شرح تعدادی از مشهورترین و متداول ترین وسایل اندازه گیری گرانروی لازم است. گرانروی سنج(ویسکومتر) مخروط و صفحه از یک صفحه و یک مخروط متحرک تشکیل شده است .صفحه کنترل کننده دماست و میتوان آن را برای دمای مورد نظر تنظیم کرد .
طرز کار این دستگاه به این صورت است که ابتدا یک قطره از رنگ مورد آزمایش در مرکز صفحه قرار داده می شود وسپس قسمت مخروطی شکل بر روی آن قرار میگیرد.
آزمایش های رنگ به سه دسته تقسیم می شوند.
· آزمایش های رنگ مایع
· آزمایش های فیلم خشک نشده رنگ
· آزمایش های فیلم خشک شده رنگ
آزمایش های کنترل رنگ تولید شده طوری طرح ریزی شده اند که با استاندارد های تعیین شده منطبق باشند.آزمایش های زیر در مورد رنگ های معمولی انجام میشوند،امّا برای محصولات استثنایی ممکن است از آزمایش های دیگری هم استفاده شود.
اندازه گیری درجه ی پخش شدن (دیسپرش شدن رنگدانه):
پخش شدن رنگدانه در رزین با وسیله ای به نام گریندومتر(Grindometer ) اندازه گیری می شود.درجه پخش شدن ، میزان پخش رنگدانه ،ریزی و درشتی آنها وبه طورکلی تمیزی رنگ را نشان می دهد. درجه پخش شدن معیاری برای کیفیت آسیب رنگ می باشد. این وسیله از یک قطعه ی فلزی مکعب مستطیل به ابعاد 17 Ï 4 Ï 1 سانتی متر تشکیل شده است. در سطح 17Ï4 سانتی متر، دو شیار طولی دیده می شوند.عمق این دو شیار از یک طرف به طرف دیگر افزایش می یابند؛ و از 0 تا 100 میکرون درجه بندی شده است.یک تیغه فلزی لبه تیز نیز برای کشیدن رنگ بر روی شیارها وجود دارد.
ابتدا قطعه مکعب مستطیل شیاردار به صورت کاملاً افقی قرار داده می شود؛چند قطره از رنگ مورد آزمایش بر روی عمیق ترین نقطه ی شیارها ریخته می شود.
سپس رنگ به وسیله تیغه ی فلزی در طول دو شیار پهن می شود. باید دقت کرد که مقدار رنگ ریخته شده برای پوشاندن همه ی طول شیار کافی باشد. به محض این که رنگ در طول شیارها پهن شد، مکعب مستطیل فلزی در مقابل نور قرار می گیرد وسطح رنگ بررسی می شود. ریزی ذرّات رنگدانه موجود در رنگ،در یک مقطع از شیار نمایان می شود.
آزمایش ذوب با سدیم (تکلیس با سدیم):
در یک لوله آزمایش پیرکس کاملا تمیز و خشک یک تکه کوچک سدیم (حدود 5 میلی متر یا به اندازه دانه عدس) بیندازید لوله را با گیره چوبی بگیرید و با استفاده از عینک ایمنی انتهای لوله را روی شعله چراغ گاز گرم کنید تا بخارات سفید از آن متصاعد شود لوله را از شعله دور کنید و حدود 10 میلی گرم از ترکیب آلی را، و در صورتی که ترکیب مایع است حدود 4 قطره از آن را، درون لوله آزمایش، دقیقا بر روی سدیم، بریزید و آن را به مدت دو دقیقه گرم کنید سپس لوله را از شعله دور کنید و 10 میلی گرم دیگر ترکیب آلی به آن اضافه کنید و دوباره انتهای لوله را گرم کنیدغالبا رنگ سرخی در ته لوله مشاهده می شود.
اکنون لوله را بگذارید سرد شود حدود 1.5 میلی لیتر اتانول به آن اضافه کنید تا بدین ترتیب سدیم اضافی حذف شود. از افزایش الکل بیشتر، اجتناب کنید. لوله آزمایش را کمی گرم کنید و به کمک یک همزن شیشه ای محتویات آن را با 20-15 میلی لیتر آب مقطر بشویید و به بشر کوچکی منتقل کنیدسپس آن را گرم کنید تا بجوشد و محلول جوشان را صاف کنید محلول صاف شده شامل یونهایی از عناصر موجود در نمونه است که هر کدام را با واکنشگر یا معرف ویژه ای تشخیص می دهیم
فرمول واکنش سدیم با یک ترکیب آلی حاوی را بنویسید؟ N, S وCl
یک میلی لیتر از محلول اولیه را با استفاده از استیک اسید اسیدی کنید (pH اسیدی با کاغذ تورنسل کنترل شود) سپس چند قطره محلول سرب استات (5%) به آن افزوده و به هم بزنید. تشکیل رسوب قهوه ای مایل به سیاه موید وجود گوگرد در ترکیب است
فرمول واکنش فوق را بنویسید؟
به 2 میلی لیتر از محلول اولیه، حدود 5-3 قطره محلول سدیم نیتروپروسیات تازه تهیه شده اضافه کنید رنگ ارغوانی مایل به بنفش موید وجود گوگرد در ترکیب است. این ترکیب پایدار نیست و کمپلکس پس از مدتی تجزیه می شودبه دو میلی لیتر از محلول اولیه چهار قطره محلول سیر شده فروآمونیوم سولفات و چهار قطره محلول پتاسیم فلوئورید 30% بیفزایید. مخلوط را حدود 45 ثانیه به آرامی گرم کنید و بجوشانید. سپس آنرا با محلول سولفوریک اسید 30% اسیدی کنید (pH اسیدی با کاغذ تورنسل کنترل شود) از افزایش اسید به مقدار بیش از حد لازم اجتناب کنید. ایجاد رسوب پتاسیم فروفری سیانید آبی رنگ (آبی پروس)، موید وجود نیتروژن در ترکیب است. چنانچه رسوب آبی مشخص نباشد، اگر محلول آبی یا آبی مایل به سبز است، آن را صاف کنید. اگر روی کاغذ صافی، آبی رنگ باشد، با اینکه جواب ضعیفی است ولی وجود نیتروژن مثبت تلقی می شود.
حل کردن و صاف کردن
بحث کلی: یکی از معمولترین روش های تهیه ترکیبات آلی خالص در آزمایشگاه حل کردن و صاف کردن می باشد. در واکنش های آلی معمولا همراه محصول اصلی واکنش، محصولات جانبی نیز تولید می شوند (Partial Decomposition). در نتیجه آگاهی از روشهای جداسازی ناخالصی ها و توجیه جسم سوم حاصل یکی از ضروریات در هر آزمایشگاهی است.
خواص فیزیکی ترکیبات ممکن است خیلی با یکدیگر متفاوت باشند و این امر اجازه می دهد که آنها را با استفاده از اختلاف حلالیت، وزن مخصوص و یا سایر خواص فیزیکی از یکدیگر جدا نمود البته بایستی به خاطر داشته باشید در آن دسته از واکنشهای آلی که همولوگ با هم تولید می شوند اختلاف در خواص فیزیکی یا شیمیایی این سری از ترکیبات بسیار جزئی است. که در بعضی روشهای جداسازی و خالص سازی به طور ناقص صورت می گیرد و با روشهای معمولی این گونه ترکیبات قابل جداسازی نیستند.
به طور کلّی ترکیبات آلی به وسیله روش های زیر جداسازی و خاص سازی می شوند:
.حل کردن و صاف کردن (Solution and Filteration)
2.استخراج (Extraction)
3.کریستاله کردن (Crystallization)
4.تصعید کردن (Sublimation)
5.تقطیر (Distillation)
6.جداسازی کروماتوگرافی (Chromatographic Separation)
روش مورد استفاده، بستگی به طبیعت مواد خواهد داشت.
1-حل کردن و صاف کردن:
بحث کلی:
در اینجا روش ما با استفاده از اختلاف حلالیت دو ترکیب موجود در یک مخلوط آنها را از یکدیگر جداسازی می نماییم. در این حالت یکی از اجزائ مخلوط به راحتی در حلال حل شده در حالیکه جزء دوم ممکن است نسبتا غیر محلول باشد. در نتیجه جزء محلول مخلوط که با تکان دادن در حلال حل شده است از جزء دوم نامحلول به وسیله صاف کردن از یکدیگر جدا می شوند.
جزء نامحلول روی کاغذ صافی و جزء محلول بعد از تبخیر حلال قابل بازیابی است. یک نمونه عملی این روش جداسازی مخلوط ماسه و شکر از یکدیگر می باشد. اگر آب را به عنوان حلال انتخاب کنیم شکر در آب حل شده در حالیکه ماسه در آب نامحلول است و پس از صاف کردن روی صافی خواهد ماند. تبخیر آب به آرامی اجازه می دهد شکر بازیابی شود.
جداسازی ترکیبات با استفاده از اختلاف حلالیت کاملا موثر و مفید خواهد بود مخصوصا اگر حلالیت جزئی که در حلال کمتر محلول است دارای وزن مخصوص کمتری نیز باشد. اگر جزء غیر محلول رسوب شود جزئی که در بالا ایستاده را با دقّت می توان جداسازی نمود. این روش بسیار موثر است مخصوصا هنگامی که یکی از اجزاء در اثر انحلال به صورت ژلاتینی در نیاید چون در این صورت صاف کردن با مشکل روبه رو خواهد شد.
در مواردیکه یکی از اجزاء به صورت معلّق است و به سختی رسوب می شود استفاده از نیروی گریز از مرکز (سانتریفیوژCentrifuge) میتواند موثر واقع شود یکی دیگر از روشهایی که در صاف کردن کمک می کند صاف کردن به وسیله خلا است (Suction Filteration) که بعدا به آن اشاره خواهد شد.
1.یک مخلوط از دو ترکیب آلی (یک گرم بنزوئیک و یک گرم شکر) تهیه نموده و سپس آن را به پنج قسمت مساوی تقسیم نمایید (سه قسمت را در آزمایش های بعدی به کار خواهیم برد).
الف) به یک قسمت 25 میلی لیتر آب مقطر اضافه نموده و به شدت تکان دهید وسپس صاف نمایید. باقیمانده روی صافی را با نمونه های هر یک از ترکیبات مقایسه کنید. حلالیت نسبی اسید بنزوئیک و شکر در آب چگونه است؟
ب) یک قسمت دیگر را در 10 میلی لیتر اتانول حل کرده م مخلوط را به شدت تکان دهید و سپس صاف کنید.باقیمانده روی صافی را با نمونه های هر یک از ترکیبات مقایسه کنید. حلالیت نسبی اسید بنزوئیک و شکر در الکل چگونه است؟